Острая почечная недостаточность - это синдром, развивающийся вследствие внезапного прекращения функционирования почек, что проявляется нарастающей азотемией, дисбалансом электролитов, метаболическим ацидозом и нарушением выделительной способности. Из этой статьи вы узнаете какие причины вызывают острую почечную недостаточность, ее симптомы, а также о том, как проводится лечение острой почечной недостаточности, и какие меры профилактики вы можете проводить, чтобы оградить ребенка от заболевания.
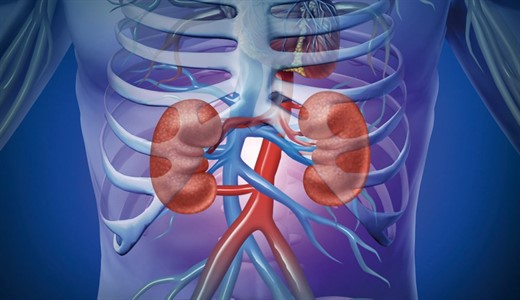
Причины острой почечной недостаточности
Нарушения реологических свойств крови, блокада микроциркуляции (гемолитико-уремический синдром (ГУС), шок), которые приводят к ишемии почечной ткани.
Гиповолемия различного генеза. Необходимо отметить, что с помощью местно вырабатывающихся биологически активных веществ почечный кровоток способен сохранять ауторегуляцию при колебаниях системного артериального давления от 30 до 160 mm Hg. Однако, дальнейшее падение показателей гемодинамики приводит к шунтированию крови на уровне мозгового вещества почек, что вызывает ишемизацию коркового слоя (снижение фильтрации). Как результат, наблюдаются переполнение кровью сосудов мозгового слоя и стаз крови в них. Вследствие этого имеет место значительный рост сопротивления локальному кровотоку, развитие отека интерстициального вещества, клеток и базальной мембраны канальцев, что влечет за собой нарушение реабсорбции и секреции. Органические изменения почечной ткани возникают при наличии артериальной гипотензии <60 mm Hg в течение 2 и более часов.
Гипоксия (респираторного генеза), на фоне которой органические нарушения в почках возникают при гипоксемии (рО2<50 mm Hg) или гиперкапнии (рСО2>90 mm Hg) в течение 8-12 часов.
Поступление (или эндогенное образование) нефротоксических ядов и лекарственных средств - ртути, кадмия, четыреххлористых углеродов, пестицидов, некоторых антибиотиков, витамина Д, лейкотоксинов, гипердоз салуретиков.
Особенностью течения синдрома ОПН является его цикличность с возможностью полного восстановления функций почек. Необходимо отметить, что этиологические особенности проявляются только в самой начальной стадии.
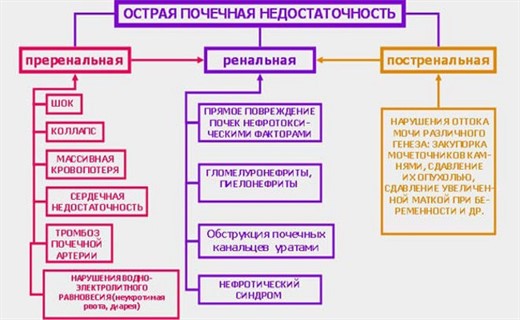
Острая почечная недостаточность - формы заболевания
- Преренальная острая почечная недостаточность у детей развивается в результате шока, обструкции почечных сосудов (тромбозы, эмболии), электролитных нарушений (острая гиперкальциемия, гипонатриемия), гемолиза и миолиза (краш-синдром, переливание несовместимой крови), эндогенных интоксикаций (кишечная непроходимость).
- Ренальная форма вызывается экзогенными нефротоксинами (ядовитые грибы, ртуть), передозировкой медикаментов (антибиотики), инфекциями (анаэробный сепсис, гемолитико-уремический синдром), отсутствием почки, осложнением гломерулонефрита и других почечных заболеваний. В возникновении постренальной формы наибольшее значение имеют аномалии развития, мочекаменная болезнь, опухоли, ятрогенные факторы (хирургическая лигатура на мочеточнике).
Развитие острой почечной недостаточности
Развитие острой почечной недостаточности (ОПН) может сопровождать различные заболевания. Она может выявляться неожиданно для пациента и врача, который должен уметь провести дифференциальную диагностику и знать принципы современной консервативной и оперативной терапии.
Образование и выведение мочи - процесс не настолько простой, как это может показаться на первый взгляд. Почечный эпителий стоит на втором месте после клеток ЦНС по ранимости под влиянием гипоксии и нарушения кровотока. Для нормального функционирования почечной ткани необходимо не менее 8 мл/мин/100 г ткани кислорода и 25 % сердечного выброса.
Мочевыделительная система принимает участие в регуляции многих функций организма:
- Регуляции водного баланса. У взрослого человека в почечных клубочках фильтруется 200 л первичной мочи, а выделяется из организма лишь 1,5 л. Необходимо отметить, что даже при стимуляции суммарное выделение жидкости через кожу, легкие и кишечник не превышает 2/3 данного объема.
- Регуляция кислотного-основного состояния (КОС). В почечных канальцах происходит синтез и экскреция кислых продуктов и реабсорбция щелочных.
- Регуляция электролитного баланса. В моче содержится сульфатов в 90 раз больше, чем в плазме. При нормальных условиях в почечных клубочках за сутки фильтруется 500 г Nа+, а выделяется его в конечном итоге всего 3 г. За сутки в почечных канальцах секретируется, а затем выводится 3-5 г К+. Выделение азотистых шлаков (около 30 г/сут). Выведение инородных веществ, среди которых различные медикаментозные средства, свободный гемоглобин, миоглобин.
- Регуляция кровообращения. В почечной ткани образуется большое количество различных биологически активных веществ, некоторые из которых носят вазоконстрикторный а некоторые - вазодилятирующий характер.
- Регуляция эритропоэза. Оказалось, что почечная ткань является основным источником эритропоэтина.
Макроскопическая ткань почки подразделяется на корковое вещество, основную часть которого составляют клубочки, и мозговое вещество, основу которого составляют почечные канальцы. Необходимо отметить, что у новорожденные соотношение толщины коркового и мозгового слоев 1:4, а у взрослых людей (начиная с пубертатного периода) - 1:2.
В клубочковых канальцах происходит фильтрация первичной мочи (фильтруется безбелковая часть плазмы, 75% миоглобина и 3% свободного гемоглобина). Экзогенное введение вазопрессоров резко снижает величину фильтрации. Подобный же эффект оказывает и использование индометацина, являющегося ингибитором простагландинов. Отрицательно на уровень фильтрации влияет и повышение иптерстициального (внутрикапсульного) давления, которое имеет место при развитии отека в ткани почки, обтурации просвета мочевыводящих путей.
Как видно из всего вышеперечисленного процесс фильтрации в почечных клубочках является пассивным, поэтому эндотельальные клетки данного региона относительно примитивны (ее имеют сложной структуры и высокого уровня метаболизма), вследствие этого их функция, а, значит, и функция клубочков при адекватном лечении должна восстанавливаться первой (по сравнению с функцией почечных канальцев).
Суммарная длина всех почечных канальцев у взрослого человека приблизительно составляет 120 км. В зависимости от расстояния от коркового слоя все канальцы делятся на проксимальные и дистальные.
Главной функцией проксимальных канальцев является реабсорбция всех веществ, попавших в первичную мочу, но необходимых для организма. Здесь реабсорбируются из фильтрата 99% воды, натрий, хлор, ионы бикарбоната, глюкоза, аминокислоты, 93% К+, 45% мочевины. Необходимо помнить о том, что новорожденные дети реабсорбируют натрий гораздо интенсивнее, чем взрослые, что обуславливает склонность к отекам у данного контингента больных, а также наличие у них гипоосмолярной мочи даже на фоне сниженного диуреза.
Секреция является одной из основных функций дистальных канальцев. В просвет канальцев из окружающих тканей секретируются органические чужеродные вещества и медикаменты, ионы водорода, кислые соли сильных кислот, ионы аммония, К+.
Необходимо отметить, что и реабсорбция и секреция - процессы активные, протекающие с большим потреблением энергии, поэтому и эпителий почечных канальцев высокоорганизован, что обуславливает медленное восстановление его функции даже на фоне адекватного лечения.
Особый интерес представляет собой проблема кровотока в почке. Его развитие и стабилизация в человеческом организме совпадает по времени с концом периода полового созревания. В ткани почки одновременно функционируют:
- клубочковый кровоток, обеспечивающий фильтрацию первичной мочи;
- канальцевый кровоток, берущий свое начало от афферентной артериолы и обеспечивающий кровоснабжение канальцев;
- мозговой кровоток, начинающийся от афферентной артериолы, образующий vasa recta реабсорбируются вещества из проксимальных канальцев, и из них забирается то, что будет секретировано в дистальной части петли Генле.
Регуляция всех трех типов кровотока происходит в основном на местном уровне. Сложность строения гемодинамического аппарата почки объясняет, почему самым частым повреждающим фактором для этого органа является ишемия.
Симптомы острой почечной недостаточности
В течении острой почечной недостаточности выделяют четыре стадии: начальную, олигоанурическую, восстановительную и выздоровление.
Стадии острой почечной недостаточности
стадия - преданурическая или стадия функциональных нарушений. На этом этапе течения острой почечной недостаточности на первое место выходит сиптоматика основного заболевания, сопровождающаяся снижением диуреза до величины, не превышающей 25-33% от нормальной или даже до анурии.
стадия - олиганурии, развивающаяся в результате прогрессирования следующих патофизиологических процессов:
- тубулонекроза,
- устойчивого спазма афферентных сосудов,
- канальцевой обструкции,
- первичного поражения эпителия канальцев и обратного всасывания фильтрата,
- снижения проницаемости капиллярных клубочков.
Именно на этой стадии начинают появляться и получают дальнейшее развитие признаки и симптомы, характерные для почечной недостаточности.
К ним в первую очередь относятся олиго- и анурия, которые, естественно сопровождаются синдромом гипергидратации. Увеличение объема жидкости сопровождается нарастанием массы тела. Одновременно с накоплением внутрисосудистой жидкости в сосудистом русле происходит снижение ее осмолярности, и вода начинает выходить в интерстициальное пространство и накапливаться в тканях. При этом увеличивается нагрузка на сердце, развиваются симптомы сердечной недостаточности, появляются отеки, жидкость накапливается в полостях.
Появляются самые разнообразные изменения в клинических анализах мочи. В крови нарастает уровень мочевины (не только из-за снижения ее выведения почками, но и в результате катаболизма) и креатитнина. Снижается концентрация белка.
В результате несоответствия между скоростью поступления в кровоток ионов калия и их выведением развивается гиперкалиемия. Клинически гиперкалиемия проявляется, главным образом, брадикардией, изменениями на ЭКГ, пароксизмальными аритмиями и может закончиться остановкой сердца. Отмечается резкая мышечная слабость, боли в животе. Необходимо отметить, что у большинства больных с ОПН, как следствие уремии, развивается полисерозит и соответственно, рвотно-диарейный синдром. Как правило, у подобных пациентов на фоне массивной рвоты и профузной диареи концентрация калия в плазме крови бывает не только не повышена, но и снижена.
Острая почечная недостаточность: клинические рекомендации
Ацидоз, одной из главных причин которого, является гиперкалиемия (повышение уровня К+ на 0,5 ммоль/л в плазме крови способствует снижению pH на 0,1) - непременный спутник ОПН. Его развитию способствуют также прекращение синтеза Н+ в почечных клубочках и высокий уровень катаболизма.
Гипокальциемия, гипохлоремия и гипонатриемия сопровождают данную патологию.Выходящий в большом количестве из клеток в сосудистое русло магний обуславливает сонливость, присущую пациентам с ОПН.
Быстро развивается анемия, вызванная снижением синтеза эритропоэтина, гипопротеинемией, нарушением утилизации железа в кишечнике и уменьшением продолжительности жизни самих эритроцитов.
В клинических анализах крови обращают на себя внимание нейтрофильный лейкоцитоз со сдвигом влево, лимфоцитопения, моноцитопения, эозинофилопения, повышение СОЭ.
Все случаи ОПН сопровождаются синдромом диссеминированного внутрисосудистого свертывания, в основном на стадии гиперкоагуляции и фибринолиза.
Артериальная гипертензия при острой почечной недостаточности встречается всего лишь в 10-15% случаев. С другой стороны, артериальная гипотония - практически постоянный признак, которым отличается острая почечная недостаточность, обусловленной экстраренальными причинами. Необходимо отметить, что стойкое снижение артериального давления может свидетельствовать о возникновении у пациента сепсиса, который может развиваться очень медленно - много часов и даже суток.
Поражения легких и плевры при острой почечной недостаточности носят разнообразный характер. Наиболее часто имеет место тахипноэ, с помощью которой организм больного пытается компенсировать развивающийся метаболический ацидоз. Проявлением уремического полисерозита выступает плеврит, иногда продуктивный, который определяется при аускультации наличием шума трения плевры или, при скоплении выпота в плевральной полости, глухостью дыхательных шумов. При тяжелой уремии часто можно видеть на рентгеновском снимке значительное усиление сосудистого рисунка в виде характерной "бабочки"; при этом над легкими выслушивается жесткое дыхание с множественными разнокалиберными влажными хрипами.
Развитие плеврита обычно происходит параллельно с появлением перикардита, который раньше называли "похоронным звоном" для пациента с уремией. Морфологически в полости перикарда имеется картина асептического воспаления с массивными отложениями фибрина. Клинически при фибринозном перикардите имеется скудная симптоматика, редко встречается болевой синдром, выслушивается нарастающий (иногда за часы) пансистолический шум трения обычно над всей поверхностью сердца, иногда проводящийся на заднюю поверхность грудной клетки.
Продолжительность олигоанурической стадии от нескольких дней до 1 месяца (крайне редко - дольше), в среднем ее продолжительность составляет 12-14 дней.
стадия - полиурическая. Она характеризуется нарастанием диуреза, что свидетельствует о восстановлении функции эпителия почечных клубочков, но не канальцев. В начале анурия сменяется олигурией, затем в течение 2-5 дней диурез нарастает настолько, что может достигать 10-12 литров в сутки (признак того, что ребсорбция еще "не работает"). Быстрого улучшения состояния больного, равно как и его самочувствия, нет. Несколько уменьшаются признаки интоксикации, выраженность ДВС-синдрома, но еще долго сохраняются анемия, астенический синдром. На этот период приходится 37% всех летальных исходов от ОПН (80% из них - от вторичной инфекции). У всех больных имеется инфекция мочевых путей. В этой стадии наиболее опасной является гипокалиемия, обусловленная полиурией.
Полиурическая стадия продолжается от нескольких дней до нескольких месяцев.
стадия - выздоровление. Характеризуется исчезновением клинических признаков почечной недостаточности, анемии, ДВС-синдрома. Однако, как правило долго наблюдается картина хронической инфекции мочевыводящих путей.
Лечение острой почечной недостаточности
Чтобы начать лечение, в первую очередь необходимо устранить действие этиологического агента: промывание желудка и введение антидотов при отравлении, восстановление гемодинамики при циркуляторных расстройствах, оперативное устранение обструкции.
- На I стадии лечения острой почечной недостаточности проводятся противошоковые мероприятия: изотонический раствор натрия хлорида 20 мл/кг и/или свежезамороженная плазма, альбумин 5%-ный - 5-10 мл/кг в течение 0,5-2 ч под контролем ЦВД; фуросемид 1-2 мг/ кг, допамин 1,5-3 мкг/кг/мин; при необходимости - плазмаферез, гемосорбция, антибиотикотерапия.
- На II стадии, когда проводится лечение острой почечной недостаточности назначаются гемодиализ, диета с пониженным содержанием белка, натрия, калия, фосфора, поддержание водного баланса, внутривенно глюкозо-солевые растворы, купирование метаболического ацидоза (гидрокарбонатом натрия), снижение азотемии (высокие сифонные клизмы с 0,9%-ным натрия хлоридом), пероральные энтеросорбенты.
Лечение острой почечной недостаточности на олигоанурической стадии - диета, обогащенная калием, кальцием, натрием, магнием, ограничение белка. Жирорастворимые витамины, мембра-нопротекторы, электрофорез с эуфиллином, никотиновой кислотой на область почек.
Как лечить острую почечную недостаточность?
Лечение острой почечной недостаточности в преданурической стадии должно быть направлено на восстановление ОЦК, снятие периферического вазоспазма, устранение гипоксии. Больному должна быть налажена ингаляция обогащенной кислородом смеси.
Инфузионная терапия проводится по следующей схеме: первоначально инфузируется объем жидкости, равный 2% от массы тела больного. В ее состав как правило включают полиионный солевой раствор и 10% раствор глюкозы с инсулином. При условии, что на подобную водную нагрузку диурез получен не был, то необходимо стимулировать его образование внутривенным введением лазикса в дозе 1 мг/кг (суточная доза может достигать 5 - 10 мг/кг). Необходимо отметить, что лазикс не только салуретик, он также улучшает микроциркуляцию в паренхиме почек. В дальнейшем продолжают инфузию, избегая применения растворов, содержащих К+. Хороший эффект в лечении дает инфузия малых доз допамина (2-5 мкг/кг/мин). С дезагрегационой целью показано использование гепарина в суточной дозе 90-100 ед/кг (под контролем коагулограммы или времени свертываемости крови по Ли-Уайту). Возможно однократное переливание свежезамороженной плазмы в объеме 10 мл/кг.
Во время проводимого лечения необходим тщательный мониторинг за параметрами гемодинамики (в том числе и ЦВД), дыхания, скоростью выделения мочи. Желательно не реже, чем 4 раза в сутки производить забор крови для определения концентраций электролитов, азотистых шлаков, белка.
Неотложная помощь при острой почечной недостаточности
При развитии стойкой анурии продолжают парентеральное ввденение лазикса (до 10 мг/кг/сут) в сочетании с инфузией донамина. Объем жидкости вводимой за сутки определяется суммированием перспирационных потерь, текущих патологических потерь и объема мочи, выделенной за предыдущие сутки. В состав инфузионной терапии входят концентрированные (15 - 30%) растворы глюкозы с инсулином, 0,9% раствор NaCl и свежезамороженная плазма. Анемию корригируют трансфузией взвеси отмытых эритроцитов. Уровень гиперкалиемии снижают введением 10% раствора глюконата кальция по 30 мг/кг, а также гидрокарбоната натрия в стандартных дозировках. Причем, необходимо помнить, что сода окажет желаемый эффект только при условии, что образующиеся молекулы СО2 будут эффективно удаляться через легкие (контроль газов крови).
Под контролем показателей свертывающей системы крови продолжают применение гепарина. Очень часто пациентам во 2 стадии острой почечной недостаточности приходится назначать антибиотики для профилактики и лечения вторичной инфекции, при этом надо помнить, что сульфаниламиды, нитрофураны и тетрациклины подобным больным противопоказаны.
Диета при острой почечной недостаточности
Питание детей с острой почечной недостаточностью является чрезвычайно важной проблемой, так как у них преобладает катаболизм. Восстановления почек требует адекватного поступления калорий для усиления энергетического метаболизма. Отмечено, что внутривенное введение эссенциальных аминокислот и глюкозы приводит к положительному азотистому балансу, улучшению репарации, поддержанию веса, снижению уровня мочевины и смягчению уремических симптомов.
При анурии, продолжающейся на фоне лечения более суток необходимо начинать проведение операции по очищению крови, вне зависимости от показателей креатинина, мочевины, калия. Могут быть использованы гемодиализ, артериовенозная гемофильтрация, гемодиафильтрация, перитонеальный диализ.
Показаниями к экстренному диализу являются:
- Анурия больше суток;
- Олигурия с гипертонией и неврологическими нарушениями;
- Повышение внутрисосудистого объема, приводящее к застойной сердечной недостаточности, отеку легких и артериальной гипертензии;
- Гиперкалиемия, неподдающаяся консервативной терапии;
- Уремическая симптоматика, выражающаяся в летаргии, неврологических нарушениях или судорогах.
Следовательно, в настоящее время решение о начале диализа не зависит от лабораторных критериев, таких как мочевина или креатинин плазмы, а больше опирается на общее состояние больных с учетом клинического течения острой почечной недостаточности.
Главным в лечении полиурической стадии острой почечной недостаточности является поддержание баланса воды и электролитов (для чего нужен тщательный мониторинг ВЭБ) и постепенное увеличение пероральной белковой нагрузки.

